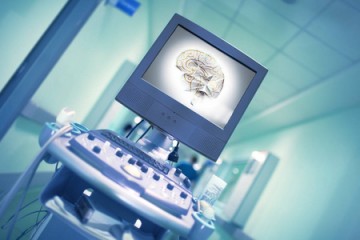
近日,创新医疗器械支持政策频出:
- 3月27日,国家药监局医疗器械技术审评中心发布《关于进一步加强对创新医疗器械支持力度有关事项的通告(2025年第3号)》,提出“定点化”加强对创新医疗器械研发指导优化。
- 3月31日,国家药监局发布《关于优化全生命周期监管支持高端医疗器械创新发展的举措》,聚焦医疗器械行业的全生命周期监管优化。
创新医疗器械研发风险高、投资大、周期长,商业化难度高。如今,两大政策从“研发端+监管端”开始倾斜,无异于让“真创新”少走弯路,避免无序竞争,推动行业健康、有序发展。
受此消息影响,4月1日,多支医疗器械ETF上涨,幅度在2%-3%之间。
01
谁的利好?
从促进行业发展角度看,政策端最关键的着重点之一,就是要与时俱进。
3月31日,国家药监局发布《关于优化全生命周期监管支持高端医疗器械创新发展的举措》(以下简称《举措》)提出重点支持四大领域:医用机器人、高端医学影像设备、人工智能医疗器械和新型生物材料。
医用机器人被列为第一项无可厚非,背后有三重驱动力。第一,从临床角度看。手术机器人有望重构现代外科医疗体系,以应用最为广泛的骨科手术机器人为例,临床数据显示,可将膝关节置换等复杂手术时间缩短30%,精度控制在亚毫米级,使患者手术麻醉时长及感染风险大幅降低。2024年,中国工程院院刊《工程》将手术机器人列为“全球十大工程成就”之一。
第二,从市场接受度看。中国正成为全球手术机器人市场增长速度最快的区域,预计至2030年,中国手术机器人的市场规模将飙升至709.52亿元,年均复合增长率达37%。特别是自2018年、2020年“配置证改革”以来,中国手术机器人市场飞速发展,甚至供不应求。据悉,截至2020年底,“2018版配置证”全国实际使用率高达96.4%,几乎达到了满负荷运行。第三,国产势力崛起。仅从产品获批数量来看,目前,国产手术机器人已全面超过进口。
据不完全统计,仅在2024年,就有超过40张针对不同细分领域的国产手术机器人获批NMPA注册证。其中,骨科手术机器人代表企业为天智航、元化智能、佗道医疗、柳叶刀、三坛医疗等国产品牌;腔镜手术机器人代表国产企业为微创医疗、精锋医疗、术锐、康多等。
“临床获益显著+市场接受度高+国产技术成熟”,从任何角度看,手术机器人都亟需建立规范化监管和研发标准。为此,《举措》提出四个方向:
一是制定医用机器人的分类指导原则,形成医用机器人命名专家共识。并且细化医用机器人、高端医学影像设备核心零部件管理要求。
二是加快推进医用机器人等领域的基础、通用标准和方法标准等制修订工作,筹建医用机器人、人工智能医疗器械标准化技术委员会。
三是细化上市后监管要求,加快制定医用手术机器人等高端产品的质量管理体系检查要点。
四是持续跟踪上市后质量监测,督促医疗器械使用单位对手术机器人等医疗器械定期检查维护,保障临床使用质量。
除手术机器人之外,《举措》还将目光投向了医疗器械行业的未来——强调加强对增材制造用医用材料、脑机接口柔性电极、基因工程合成生物材料等新型生物材料的标准化研究,为下一代技术发展筑牢根基。
厘清真正的创新
3月27日,国家药监局医疗器械技术审评中心发布《关于进一步加强对创新医疗器械支持力度有关事项的通告(2025年第3号)》(以下简称《通告》),明确通过“提前介入、一企一策、全程指导、研审联动”机制,加速创新医疗器械审评审批进程。
对于创新医疗器械,《通告》明确建立临床试验方案预审查机制:申请人完成临床前研究及可行性试验后,可通过专用通道提交临床试验方案、立题依据综述等材料,审评中心将出具预审查意见作为后续审评依据。这一机制将审评时间前移,降低研发风险。
对于非创新医疗器械,《通告》要求企业严格参照《医疗器械临床评价技术指导原则》等文件开展临床评价,确保数据科学性与充分性。此举旨在压缩低水平重复研发空间,引导资源向真正具有临床价值的创新领域倾斜。
与此同时,为了进一步释放“合规信号”,《通告》强调企业应以临床需求为导向设计开发,确保提交资料真实、完整、可追溯,承担相应法律责任。
03
顶层设计引导创新倾斜
今年开年(1月3日),国务院发布《关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见》(以下简称《意见》)。“先药后器械”,继创新药领域的两份重要政策《关于医保支持创新药高质量发展的若干措施(第二轮征求意见稿)》和《关于完善药品价格形成机制的意见(征求意见稿)》后,创新器械的系列支持政策被提上日程。开篇所述的两份文件,正是该项顶层设计在医疗器械端的延续。>不过,不同的政策节奏也体现出不同的产业进程。显然,创新药已经“进化”到了支付和定价环节,而创新器械的发力点仍着眼于监管和研发环节,支付和定价层面支持政策未来有待进一步更新。
“打造有全球竞争力的创新生态”,隐含在《意见》的字字句句:
-
到2027年,药品医疗器械监管体系、监管机制、监管方式更好适应医药创新和产业高质量发展需求,创新药和医疗器械审评审批质量效率明显提升。
-
到2035年,药品医疗器械质量安全、有效、可及得到充分保障,医药产业具有更强的创新创造力和全球竞争力,基本实现监管现代化。
全球化竞速时代,后来者必须争之于毫厘之间,政策端也为此而“卷”——《意见》特别提出,进一步缩短医疗器械临床试验审评审批时限,由60个工作日至30个工作日。
减少不必要的流程冗余、缩短产品从研发到上市的时间周期、让有临床价值的成果更快地推向市场……围绕创新医疗器械全链条的所有支持,都在逐步兑现,支付端也“有所松动”。就在昨天(3月31日),根据国家医保局发布的《神经系统医疗服务价格项目立项指南》,湖北省医保局发布了全国首个脑机接口医疗服务价格,这意味着对于所有高端创新器械而言,过去长达数年的各省立项、定价环节,有望大大缩减。这一消息的出现,远不止一次“定价动作”那么简单。重要的是医保的支持态度,对于所有创新器械,都是一个鼓舞。
【来源:MedTrend医趋势】